<2007-3회> <06/08 1차 수정> 문제:300kg 전분(녹말)을 산 가수분해할 때 이론적으로 생성되는 포도당의 양을 구하라. (산으로 분해하려면 어차피 수용액 상에서 반응하므로 가수분해 과정과 같다.) 먼저 녹말이 무엇인지 알아야 한다.

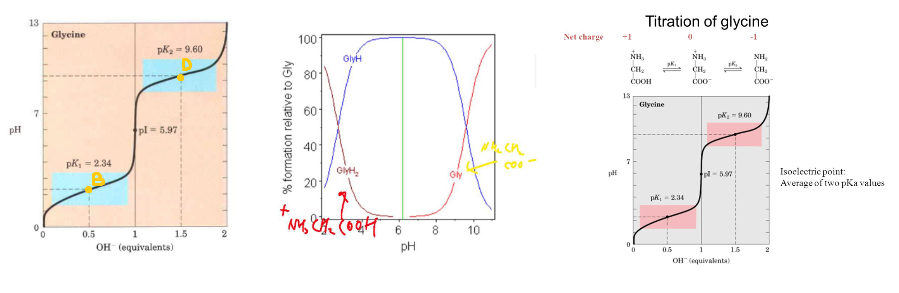
위의 사진에 찍힌 두개의 분자는 모두 녹말이다. 차이는 왼쪽은 D-glucose가 α-1,4결합 및 α-1,6결합으로 구성된 아밀로펙틴으로 오른쪽은 D-glucose가 α-1,4결합으로 구성된 녹말이다. 모두 포도당로만 구성되어 있으므로 완전히 가수 분해하면 포도당”만 “생성될 것이다.실제로 녹말의 분자량은 정확히 알 수 없다. 녹말에 포도당이 몇개 있는지 정해지지 않았다. 오른쪽 사진만 봐도 오른쪽 아밀로오스는 300~600개의 포도당으로 구성됐다는 표시만 나온다. 정확히 몇개는 모른다.그러나 녹말 분자량이 모르니까 문제를 틀리는 것은 아니다. 녹말일 수 있는 원리를 이해하면 된다.녹말은 포도당이 매우 많이 결합한 다당류이다. 이때 포도당끼리 결합할 때 물 한 분자(H2O1개)가 빠지고 결합한다. 이를 탈수 축합 반응이라는. 물이 빠져나가면서(무수)결합한다(응축)반응이라는 뜻이다.쉽게 포도당 2가지가 결합된 maltose를 보자. maltose의 분자량은 342g/mol이다. 분자량 180개의 포도당 2개가 결합하면 360에 되어야 하는데 포도당끼리 결합하면서 물이 빠지고 18을 뽑아야 할 것이다. 그래서 maltose의 분자량이(360-18)g/mol이다.그렇다면 반대로 녹말이 분해될 때는 물이 첨가되는 것이 당연한 것이다. 그렇다면 다음과 같은 반응식을 쓸 수 있다.(C6H10O5)n+nH2O→(C6H12O6)n(단, n은 많은 수)162n+18n→ 180n*C6H10O5자체는 녹말의 화학식은 아니다. 또 전분의 분자량이 162g/mol이 아니다. 녹말 자체가 포도당이 여럿 모여서 만들어지지만 포도당 분자량 180g/mol보다 작은 것은 없다.*(C6H10O5)n인 이유:전분은 포도당끼리 축합하여며 물을 하나씩 꺼내서, C6H12O6이 결합하고 H2O하나가 빠진 형태인 C6H10O5이 n분자 결합한 형태이다. *밑그림을 보자. 대괄호 안에 있는 분자의 C, H, O개수를 세다.(그림에서 H가 숨어 있지만 탄소 원자와 결합한 수소 원자는 일반적으로 표기를 생략한다. 그래서 생략된 수소 원자까지 모두 세어 줘야 한다.)

(C6H10O5)n+nH2O→(C6H12O6)n상식에서 주제:(162n+18n)g(or kg), 우변:(180n)g(or kg)의 질량 비율이 성립된다. 또, 좌변과 우변의 각 원자의 수는 일치해야 한다. (일치하는지 체크하고 보세요.)즉, 우리가 원하는 녹말의 가수 분해 반응으로 녹말과 포도당의 질량 비율만 따지면 162n:180n이 성립된다. 물의 질량은 따질 필요가 없다. 원하는 것은 전분과 포도당만 질량 관계니까.그러므로(162n)kg:(180n)kg=300kg:xkg계산 과정에서 n는 약분되므로 x=333.3kg이다.즉, 녹말 300kg을 모두 가수 분해하면 333.3kg분량의 포도당이 얻을 수 있다.(원래 녹말보다 많은 양이 생성되는 이유:물이 첨가되는 분해이므로(가수 분해)*문제로 역시”이론적인 “생성량을 물어봤다. 녹말이 산(가수)분해되어 포도당”만 ” 만들었다고 가정하는 것이다. 강산을 처리하고 가수 분해할 경우 포도당의 과잉 분해를 통한 레브 인산, 폼산 등이 생성된다. 이들은 포도당이 아니어서 가수 분해된 수량에 넣지 않다.